Una reacción química es el proceso en el que una o más sustancias se transforman en otras sustancias diferentes (los productos de la reacción). Un ejemplo de reacción química es la formación de óxido de hierro producida al reaccionar el oxígeno del aire con el hierro. Dentro de las reeacciones químicas encontramos a las reacciones exotérmicas y endotérmicas.
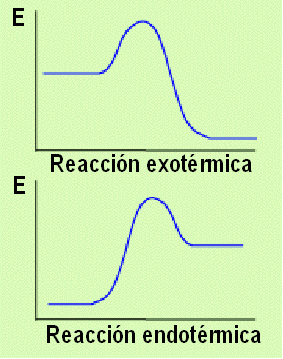
Reacción exotérmica:
Se denomina reacción exotérmica a cualquier reacción química que desprende energía, es decir con una variación negativa de entalpía.
- Se da principalmente en las reacciones de oxidación. Cuando ésta es intensa puede dar lugar al fuego. Cuando reaccionan entre sí dos átomos de hidrógeno para formar una molécula, el proceso es exotérmico.
Reacción endotérmica:
Se denomina reacción endotérmica a cualquier reacción química que absorbe energía, con una variación de entalpía positiva, osea, que tiene un incremento de entalpía. Es decir, la energía que poseen los productos es mayor a la de los reactivos. Ejemplos de estas reacciones son:
- La fotosíntesis (en este enlace pueden ver mas acerca de la fotosíntesis neetescuela)
- Reacción entre el cloruro de cobalto y el cloruro de tionilo: El agua de la cristalización del Cloruro de Cobalto reacciona con el Cloruro de Tionilo y produce Ácido Clorhídrico y Dióxido de Azufre. La reacción ocurre espontáneamente dada la gran cantidad de productos generadores de gas y por lo tanto el desorden del sistema se incrementa.

reacción endotérmica Vía: rincondelvago

