Las propiedades coligativas son propiedades que dependen sólo del número de partículas de soluto en la disolución y no de la naturaleza de las partículas de soluto (si son moléculas, atómos o iones). Las propiedades coligativas son la disminución de la presión de vapor, la elevación del punto de ebullición, la disminución del punto de congelación y la presión osmótica. Debe considerarse que las disoluciones para las cuales se estudian las propiedades coligativas serán relativamente diluidas; para concentraciones menores a 0,2 molar.
En esta oportunidad se trata de la elevación del punto de ebullición. El punto de ebullición de una disolución es la temperatura a la cual su vapor de presión iguala a la presión atmosférica externa. Debido a que la presencia de un soluto no volátil disminuye la presión de vapor de una disolución, también debe afectar el punto de ebullición de la misma.
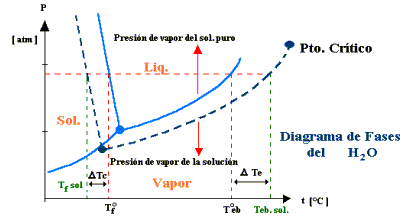 Obsérvese el diagrama de la izquierda. Debido a que a cualquier temperatura la presión de vapor de la disolución es menor que la del disolvente puro, independientemente de la temperatura, la curva líquido-vapor para la disolución siempre está por debajo de la del disolvente puro. Como consecuencia, se necesitará una mayor temperatura para igualar la presión de vapor con la presión atmosférica, y por ende, el punto de ebullición de una disolución será mayor que la del disolvente puro.
Obsérvese el diagrama de la izquierda. Debido a que a cualquier temperatura la presión de vapor de la disolución es menor que la del disolvente puro, independientemente de la temperatura, la curva líquido-vapor para la disolución siempre está por debajo de la del disolvente puro. Como consecuencia, se necesitará una mayor temperatura para igualar la presión de vapor con la presión atmosférica, y por ende, el punto de ebullición de una disolución será mayor que la del disolvente puro.
